Rubí A. Hernández Carrillo, Eduardo M. Sánchez-Cervantes
Resumen
En los últimos años ha crecido enormemente el interés por el desarrollo de nuevos dispositivos de generación de energía limpia y eficiente, las celdas de combustible se vislumbran como posibles candidatos principalmente en el área automotriz y de tecnología portátil. La clave para que se logre un avance importante se encuentra en la investigación de nuevos y mejores materiales a fin de mejorar los dispositivos ya existentes. En el laboratorio de Materiales para la Conversión y Almacenamiento de Energía de la Facultad de Ciencias Químicas de la UANL, se trabaja en la búsqueda de nuevos compuestos que puedan ser aplicados como electrolitos en Celdas de combustible tipo PEM de alta temperatura.
Introducción
Hoy en día el cambio climático y sus consecuencias sobre nuestro planeta ha impulsado el desarrollo de fuentes alternas de energía con el fin de sustituir a los combustibles fósiles. Durante las últimas décadas las llamadas energías renovables son consideradas como alternativas viables para contribuir al futuro energético con bajo impacto ambiental, así mismo el creciente avance tecnológico ha promovido la investigación de métodos de producción, almacenamiento y conversión de energía de forma limpia y descentralizada. Una de las tecnologías que están en constante evolución son las celdas de combustible (CC), estas son dispositivos electroquímicos que convierten la energía liberada en reacciones químicas directamente en energía eléctrica, de manera similar a como lo hacen las baterías o pilas que usamos habitualmente, pero la diferencia principal es que las celdas de combustible mantienen un suministro constante de electricidad siempre que exista aporte de combustible, mientras que las baterías cesan su producción cuando se agotan los reactivos químicos que contienen.
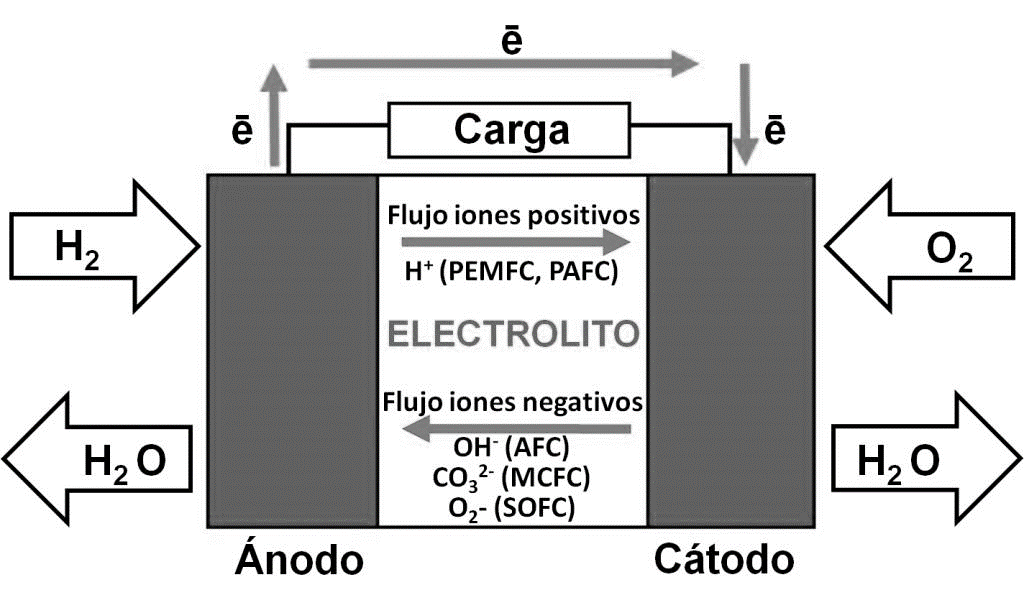
A grandes rasgos, las CC se conforman por dos electrodos, un ánodo y un cátodo, los cuales están separados por un electrólito (Figura 1). Estos dispositivos son alimentados con hidrógeno por el lado anódico y oxígeno por el lado catódico, en el ánodo el H2 se disocia en protones y electrones. Los protones son transportados a través del electrolito hacia el cátodo mientras que el electrón lo hace a través de un material conductor externo produciendo energía. Al final de su camino ambos, electrón y protón, se reúnen en el cátodo donde ocurre la reacción de reducción del oxígeno para formar agua. Así, este proceso produce agua tanto en fase vapor como líquida, corriente eléctrica y energía térmica la cual puede ser aprovechada en sistemas de cogeneración (Figura 1).
Figura 1. Funcionamiento de una celda de combustible.
Entre los beneficios que presentan este tipo de dispositivos frente a otras fuentes de generación de energía se encuentran las altas eficiencias que pueden alcanzar (entre 50% y 85%) además, su construcción puede realizarse de manera que provean el voltaje, la carga y la potencia deseada dependiendo de la aplicación para la cual fueron diseñadas. Otros de los beneficios es que sus costos de mantenimiento son bajos por lo que se ha estimado un ahorro en el costo de servicio eléctrico entre un 20 y 40% comparado con los motores de combustión interna.[1] Finalmente y a pesar de que admiten combustibles variados, con mayor o menor pureza, la emisión de gases contaminantes hacia la atmósfera es muy baja.
Las celdas de combustible son en realidad una familia de tecnologías que pueden operar a diferentes temperaturas según sea el fin para el cual estarán destinadas. Por ello se puede hablar de celdas de combustible de alta temperatura, las cuales operan a temperaturas mayores a 200 °C y las de baja temperatura, cuya operación se debe llevar a cabo por debajo de los 100 °C[2]. (Tabla I)
Tabla I. Clasificación de las celdas de combustible.
Una diferencia derivada de la temperatura de operación es el tipo de electrolito que debe utilizarse en la celda pues la efectividad del proceso electroquímico dependerá de la capacidad que tenga dicho componente para crear la reactividad necesaria para el transporte de iones.De esta gran gama de dispositivos, las Celdas de Combustible de Membrana de Intercambio de Protónico (PEMFC) son las que ofrecen mejores perspectivas a futuro para su aplicación dentro del campo de la industria automotriz y la energía portátil.Hoy en día, el electrolito más utilizado en celdas PEM consta de un polímero perfluorosulfonado conocido comercialmente como Nafion®, sin embargo para que este material funcione adecuadamente necesita operar en condiciones de elevada humedad lo que limita la temperatura de operación de la celda a 100 °C, esto trae consigo diversas problemáticas como lo es el uso de catalizadores de Pt lo que incrementa el costo de manufactura del dispositivo, además al trabajar a estas temperaturas es necesario utilizar combustibles con alto grado de pureza a fin de evitar el posible envenenamiento de los electrodos con monóxido de carbono. Es por esto que el desarrollo de nuevos materiales capaces de conducir protones a mayor temperatura sin comprometer su estabilidad térmica y mecánica, es uno de los grandes retos científicos en este campo de la investigación.
La familia de los polibenzimidazoles constituye un grupo de materiales atractivos para ser aplicados como electrolitos poliméricos en PEMFC. De dichos compuestos el poli(2,5-benzimidazol) (ABPBI) es el que presenta la estructura molecular más sencilla por tal motivo ofrece una mayor concentración de grupos funcionales que favorecen la conductividad de protones a través de la membrana[3-4].Por tal motivo, nuestro grupo de investigación se planteo el desarrollo de un nuevo electrolito polimérico a base de poli(2,5-benzimidazolio) (ABPBI) impregnado con una solución de ácido fosfórico y líquido iónico dihidrógenofosfato de 3-butil-1-etilbenzimidazolio el cual presentará propiedades químicas, térmicas y de conductividad iguales o superiores al Nafion® en PEMFC de alta temperatura (>100°C).
Con la finalidad de hacer investigación de manera sustentable, poco a poco van emergiendo nuevos compuestos amigables con el medio ambiente un ejemplo de ello son los líquidos iónicos. El principal atractivo de estos materiales es que son sales liquidas en un amplio intervalo de temperaturas, incluyendo la temperatura ambiente, debido a que están formadas por iones asimétricos de gran tamaño [5]. La elección adecuada de los iones determinará las propiedades fisicoquímicas del líquido iónico con lo cual se puede diseñar el compuesto más apropiado para cierta aplicación. Así, estos líquidos iónicos muestran baja presión de vapor por lo que se les considera disolventes no volátiles, esta característica es la base del gran interés que suscitan estos compuestos en la “química verde” para reemplazar a los disolventes orgánicos convencionales. Otras de sus características es que presentan alta estabilidad térmica (> 450 °C en algunos casos), elevada conductividad iónica (10-2–10-1 S/cm) y una amplia ventana de potencial (2-5 V) lo que los hace atractivos candidatos para aplicarse en diferentes dispositivos electroquímicos [6]. Recientemente la incorporación de líquidos iónicos en membranas poliméricas de PEMFC´s se esboza como una estrategia inteligente para incrementar la conductividad protónica y la resistencia termomecánica del polímero.
Por todo lo anterior, nuestro grupo de investigación se planteó el desafío de desarrollar una membrana de intercambio protónico basada en ABPBI impregnado con ácido fosfórico y líquido iónico dihidrógenofosfato de 3-butil-1-etilbenzimidazolio con la finalidad de generar un material con mejores propiedades químicas, térmicas y de conductividad que las mostradas por Nafion®, a manera de que puedan operar en celdas de combustible tipo PEM de alta temperatura.
Resultados y discusión
Para la obtención de las membranas[7], primero se realizó la síntesis del líquido iónico y del polímero ABPBI. Acto seguido se realizó la inmersión de las membranas en baños de dopaje, los cuales contenían H3PO4 y líquido iónico dihidrógenofosfato de 3-butil-1-etilbenzimidazolio en diferentes proporciones (Tabla II). Una vez transcurrido el tiempo de inmersión (24 horas)las membranas se caracterizaron estructural, térmica y electroquímicamente.
Tabla II.Proporción de H3PO4 y BuEtBimH2PO4 en los baños de dopaje.
|
|
Muestra |
% BuEtBimH2PO4 |
ml H3PO4 |
ml BuEtBimH2PO4 |
|
|
|
1 |
0 |
15 |
0 |
|
|
|
2 |
25 |
11.25 |
3.75 |
|
|
|
3 |
50 |
7.5 |
7.5 |
|
|
|
4 |
75 |
3.75 |
11.25 |
|
|
|
5 |
100 |
0 |
15 |
Con el uso de la técnica de espectroscopia de infrarrojo fue posible analizar los materiales preparados. En los espectros resultantes se observa la interacción entre el H3PO4 y el anillo de imidazol del polímero en la zona comprendida de 4000 a 2000 cm-1. En el rango entre 3000 y 2500 cm-1 se observa la aparición de una banda muy ancha debido a la formación del enlace N+-H, originada por la por la protonación de la imina en el ABPBI [8].Por otro lado, es posible asignar dos bandas principales debidas a la tensión O-H del ácido fosfórico y al del grupo dihidrógeno fosfato del LI. La primera de ellas aparece alrededor de 2700 a 3000 cm-1 y se encuentra solapada con la tensión N+-H. La segunda banda está centrada en 2350 cm-1. Finalmente las bandas atribuibles al ácido fosfórico libre, aparecen en alrededor de los 1250 y 850 cm-1[9].La presencia de las bandas correspondientes a los grupos funcionales de los tres componentes del sistema nos habla de la afinidad que existe entre ellos al combinarse en la membrana (Figura 2).
Figura 2. FTIR de las membranas después del dopaje.
La estabilidad térmica de nuestros materiales se probó mediante análisis termogravimétrico, el termograma revela que las membranas pierden humedad desde el principio del análisis hasta cerca de 150 °C, después de esta temperatura el peso permanece prácticamente constante hasta los 400°C, cabe mencionar que la descomposición total del polímero ocurre a los 550°C y que en el caso de estas muestras en particular, la estabilidad termal estaba fuertemente ligada con la estabilidad del líquido iónico dihidrógenofosfato de 1-butil-3-etilbenzimidazolio (Figura 3).
Figura 3.Análisis termogravimétricos de las membranas preparadas.
El último parámetro que fue analizado, en este trabajo, fue la conductividad protónica de las membranas y de esa manera evaluar el efecto de la adición del H3PO4 y líquido iónico sobre dicha propiedad. Para ello se empleó la técnica de espectroscopia de impedancia. Las mediciones solo se realizaron en las muestras que presentaron mayor resistencia mecánica, desde temperatura ambiente (aproximadamente 30 °C) hasta 150 °C. En el análisis se observó que la conductividad iónica de las membranas ABPBI-H3PO4-LI se incrementó después sumergirlas en los baños de dopaje. La conductividad más elevada fue detectada por encima de los 100°C en una muestra de polímero dopada con 50%LI-50%H3PO4 y corresponde a un valor por encima de 10-4 S/cm, resultado que se considera aceptable para materiales poliméricos con aplicación como electrolito en PEMFC y que además tiene la ventaja de operar a temperaturas superiores a 100°C.Otro dato importante que arroja este análisis es que por debajo de los 100 °C predomina un mecanismo de conductividad tipo «salto» esto es que el trasporte protónico consiste en un ágil reagrupamiento de las uniones químicas en una cadena larga de moléculas de agua, la movilidad protónica por medio de este mecanismo es mucho más rápida y se ve favorecida por la presencia de humedad en la membrana. A temperaturas superiores a 100°C cobra importancia un mecanismo vehicular de conductividad ya que la difusión de las cargas se da con mayor facilidad al incrementar la temperatura por tanto la movilidad de los protones se ve incrementada(Figura 4).
Figura 4.Conductividad de las membranas dopadas en función de la temperatura.
Conclusiones
La adición de una mezcla de líquido iónico a una membrana de ABPBI mejora significativamente su estabilidad térmica y conductividad iónica, pudiendo obtener materiales estables hasta los 200 °C con conductividades superiores a 10-4 S/cm. Aun y que los resultados son gratamente prometedores hay que seguir en la investigación con tal de que en un futuro puedan ser aplicados como electrolitos en celdas de combustible tipo PEM de alta temperatura.
Referencias.
1. Cano Castillo Ulises. Las celdas de combustible: verdades sobre la generación de electricidad limpia y eficiente vía electroquímica. Boletín IIE. (sep-oct):208-215. 1999.
2. EG&G Services for the U.S. Departament of Energy. DOE/NETL-2002/1179. Fuel Cell Handbook. 5° ed. 2002.
3. Asensio J A, Gómez–Romero P. Recent developments on Proton Conducting poli(2,5-benzimidazole) (ABPBI) membranes for high temperature polymer electrolyte membrane fuel cells. Fuel Cell. 5(3):336-343. 2005.
4. Asensio J A, Sánchez Eduardo M y Gómez–Romero P. Proton-conducting membranes based on benzimidazole polymers for high-temperature PEM fuel cells. A chemical quest. Chemical Society Reviews 39:1-30. 2010.
5. Mun J, Sim H.Handbook of Ionic Liquids: Properties, Applications and Hazards. Ed. Nova. 1a ed. ISBN: 978-1-62100-477-6.2012.
6. Romero Salvador Arturo. Líquidos iónicos a temperatura ambiente: un nuevo medio para las reacciones químicas. Rev.R.Acad.Cienc.Exact.Fís.Nat. 102(1): 79-90. 2008.
7. Hernández-Carrillo R A, Suarez-Guevara J, Torres-González L C, Gómez-Romero P, Sánchez EM “Incorporation of benzimidazolium ionic liquid in proton exchange membranes ABPBI-H3PO4” Journal of Molecular Liquids, 181:115-120 (2013).
8. Bouchet R, Siebert E. Proton Conduction in Acid Doped Polybenzimidazole. Solid State Chemistry. 118(3-4): 287-299. 1999.
9. Guerra G, Choe S, Williams D J, Karasz F E, MacKnight W J. Fourier Transform Infrared Spectroscopy of Some Miscible Polybenzimidazole/Polyimide Blends. Macromolecules. 21():231-234. 1988.