Doctor Hugo Alberto Barrera Saldaña
M.C. Gregorio Antonio Alcázar González
IBT Jonathan Saúl García Pérez
M.C. Carmen Yazmín Muñoz Mejía
M.C. Diana Raquel Rodríguez Rodríguez
Laboratorio de Bioanálisis Genómicos de Vitagenesis, S.A. de C.V.
REVOLUCIÓN TECNOLÓGICA EN EL DIAGNÓSTICO DE LABORATORIO
Las ciencias de la salud se han visto beneficiadas por oleadas de tecnologías disruptivas, que, a partir del último cuarto del siglo pasado, han acelerado su progreso. Ejemplos espectaculares han sido la que vio la luz a inicios de la década de 1970, para hacer posible la clonación de genes (la ingeniería genética con la que entre otros se produjo insulina recombinante), y la que irrumpió hacia mediados de la década de 1990, para echar abajo el dogma de la imposibilidad de clonar animales (el famoso caso de la oveja Dolly). Si bien la primera pareció una consecuencia de los avances de la época, la segunda tomó de sorpresa al mundo.
En este primer cuarto de siglo del nuevo mileno, enfrentamos un panorama similar, en el que las ciencias genómicas buscan afanosamente convertir sus proezas (el epítome es la secuenciación del genoma humano) en, por ejemplo, estuches diagnósticos para un “check up” genético, consistentes en laminillas de microscopio portadoras de detectores de secuencias de genes (chips de ADN o microarreglos de ADN, ver abajo), que permiten tipificar estos (genotipado) para revelar con una precisión sin parangón, el riesgo de cada individuo de padecer enfermedades complejas y su capacidad de responder a tratamientos con fármacos (medicina personalizada).
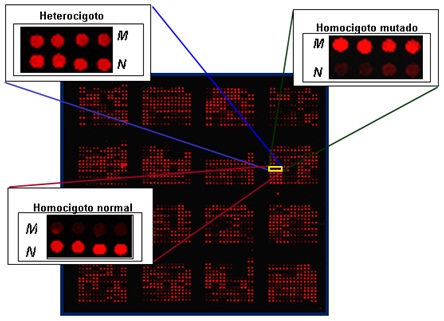
Un DNAchip o microarreglo es un soporte sólido (ver Figura 1) que contiene miles de pequeñas gotitas secas que depositan sendas sondas en la forma de fragmentos sintéticos de DNA de cadena sencilla (referidos como oligonucleótidos), inmovilizados o unidos en la superficie de la laminilla de microscopio, en posiciones fijas. Este orden preestablecido determina la variación génica en el DNA de un individuo en particular, que cada sonda está revelando. Una de las aproximaciones es hacer reaccionar (hibridar) el DNA chip en cuestión, con fragmentos de DNA procedentes de la muestra de la persona en estudio, amplificados mediante la técnica de la reacción en cadena de la polimerasa (referida como PCR) y marcados con una molécula fluorescente.
Al iluminar el microarreglo con el láser, es posible identificar a qué secuencias se ha unido la muestra problema, y discriminar específicamente entre un paciente sin mutaciones (homocigoto normal), de aquél con el gen en un cromosoma mutado y en el otro íntegro (heterocigoto), así como de aquél con ambas copias del gen mutadas (homocigoto mutado); para todos los genes que son analizados.
Figura 1. Imagen de un microarreglo iluminado con el láser. Se ilustran tres tipos de resultados: cuando el ADN del paciente reacciona tanto con los detectores para la versión “normal”, como con la “mutada” de una clase particular de gen que es rastreado (arriba a la izquierda); cuando únicamente lo hace contra la versión M de éste (arriba a la derecha); y; por último, cuando lo hace exclusivamente contra la versión N del mismo (abajo); los genotipos revelados son heterocigoto, homocigoto “mutado” y homocigoto “normal”, respectivamente.
HERRAMIENTAS GENÓMICAS PARA EL CUIDADO DE LA SALUD
Los DNAchips son, quizás, las herramientas más poderosas de esta nueva biotecnología, y el servicio diagnóstico basado en ellos ya está disponible, a costos cada día más accesibles para las clínicas y hospitales del país que lo soliciten*. Una muestra representativa de ellos sigue a continuación.
AMNIOCHIP
|
|
El AMNIOchip es un dispositivo de diagnóstico prenatal ampliado, basado en la tecnología de microarreglos de Hibridación Genómica Comparativa (aCGH, en inglés). Constituye una innovadora técnica de citogenética molecular, que examina áreas del genoma humano, evaluando la pérdida o ganancia de regiones cromosómicas, con una resolución cientos de veces superior al cariotipo tradicional (que sólo detecta alteraciones mayores de cinco millones de bases). Dicha prueba se basa en la hibridación competitiva de dos DNAs, la muestra por estudiar y una referencia, marcadas con diferente fluorocromos. Estos DNAs se hibridan sobre el DNAchip que contiene miles de diferentes segmentos de DNA humano.
Los segmentos de DNA, también denominados sondas, que están impresos en el cristal, son seleccionados a partir de diferentes bases de datos, en función de su posición en el genoma humano. Las regiones seleccionadas en el AMNIOCHIP pertenecen a regiones del genoma humano involucradas en más de 150 síndromes ya conocidos. Después, un software informático analiza la señal de fluorescencia para cada fluorocromo, buscando áreas de hibridación diferencial entre el paciente y el control del DNA, indicando por tanto la existencia de una alteración en la dosis de DNA (deleción o duplicación).
LIPOCHIP
El LIPOchip es el primer DNAchip que puede identificar de forma inequívoca las mutaciones causantes de la hipercolesterolemia familiar (HF). La HF es una enfermedad tratable y, sin embargo, cada año es causa de centenares de miles de muertes evitables en el mundo. Esto se debe a que la HF está ampliamente infra-diagnosticada e infra-tratada, pese a que con unas pruebas genéticas precoces y eficaces, los pacientes pueden recibir el tratamiento correcto y con ello superar los efectos del mal.
Las causas de la HF son genéticas, y el principal blanco o diana es el gen receptor de las lipoproteínas de baja densidad (LDLR). Normalmente, la proteína codificada por éste ayuda a eliminar el colesterol de la circulación sanguínea. Sin embargo, existen variaciones en el mismo que interfieren en el aclaramiento y que pueden dar lugar a que los niveles plasmáticos de colesterol LDL aumenten en exceso. Los niveles elevados de colesterol en la sangre dan lugar a lesiones ateroscleróticas y finalmente a placas ateroscleróticas.
PHARMAchip
El PARMAchip es una herramienta para predecir la respuesta a fármacos para mejorar la seguridad y la eficacia de las pautas de tratamiento. PHARMAchip pone de manifiesto la capacidad de un paciente de metabolizar más de 50 fármacos, proporcionando un fenotipo de: i) Enzimas de fase I (citocromo P450). ii) Enzimas de fase II (transportadores de fármacos). iii) Receptores de neurotransmisores. iv) Otras dianas farmacológicas.
Con dicha información, la fármacogenética revelada para cada individuo podrá utilizarse para:
- · Limitar su riesgo de sobredosis o de efectos adversos a los tratamientos que reciba.
- · Adaptar las dosis de sus tratamientos a su perfil de metabolización.
- · Determinar más rápidamente la dosificación terapéutica de los fármacos que le prescriban.
HEALTHIA
El análisis genético facilita detectar muy precozmente la vulnerabilidad particular de cada individuo y, al mismo tiempo, posibilita dar base científica a un tratamiento que deja de ser empírico y generalista para ser objetivo, ya que se formula de acuerdo con los principios de la medicina personalizada.
HEALTHIA es un DNAchip de genotipado, diseñado para la detección de 69 polimorfismos de un solo nucleótido o SNPs en 49 genes relacionados con patologías asociadas al envejecimiento, a la capacidad metabólica, a los mecanismos de defensa naturales frente al estrés oxidativo, y a la respuesta general a fármacos, con el objetivo de determinar el riesgo genético global de un sujeto a desarrollar una patología asociada al envejecimiento. El test se basa en la combinación de riesgos genéticos particulares para desarrollar patologías comunes asociadas al envejecimiento (Figura 2). Dichos riesgos genéticos particulares se determinan a partir de los resultados obtenidos del genotipado simultáneo de estos 69 SNPs.
Figura 2. Resultados de la valoración genética. Se ilustra un ejemplo de los resultados que se pueden obtener del estudio realizado con HEALTHIA. Desde un punto de vista genético; mientras más se acerque a la valoración “ALTA” ésta significará que se encontraron mutaciones que pudieran tener trascendencia en el desarrollo de enfermedades referenciadas.
CONCLUSIONES
México empieza a ser partícipe del uso de tecnologías de vanguardia en biotecnología genómica, en el área de la salud humana, como lo son los DNAchips, que brindan a los médicos especialistas la gran oportunidad de pronosticar el riesgo de desarrollo y posible evolución de enfermedades; de predecir su tratamiento farmacológico más adecuado, así como también de reducir los riesgos, mejorando la calidad de vida de los pacientes.
AGRADECIMIENTOS:
A los pacientes, por su solidaria participación en estos estudios; a los médicos e instituciones colaboradoras, por sus invaluables apoyos, facilitándonos muestras de los pacientes; a Progenika Biopharma, por compartirnos su experiencia sobre los microarreglos de diagnóstico; a GenetadiBiotech, por su contribución de tecnología y aportación de conocimiento sobre cariotipos moleculares, y al Fondo de Cooperación Internacional Unión Europea–México (FONCICyT), por hacer posible en parte nuestra incursión en la Fármacogenómica.
Literatura Consultada
1. Relling MV, Hoffman JM. Should pharmacogenomic studies be required for new drug approval? ClinPharmacolTher. 2007; 81(3):425-8.
2. Weinshilboum R. Inheritance and drug response. N Engl J Med. 2003; 348(6):529-37.
3. Mahgoub A, Idle Jr., Dring IG, Lancaster R, Smith RL. Polymorphic hydroxylation of debrisoquine in man.Lancet.1997; 2:584-6.
4. Eichelbaum M, Spannbrucker N, Steincke B, Dengler HJ. Defective n-oxidation of sparteine in man: a new pharmacogenetic defect. Eur J ClinPharmacol. 1979; 16:183-7.
5. DaudénTello E. Pharmacogenetics I. concept, history, objectives and areas of study. ActasDermosifiliogr. 2006; 98(1):3-13.
6. 21. Sánchez-Corona J, Flores-Martínez SE, Machorro-Lazo MV, Galaviz-Hernández C, Morán-Moguel MC, Perea FJ, Mújica-López KI, Vargas-Ancona L, Laviada-Molina HA, Fernández V, Pardío J, Arroyo P, Barrera H, Hanson RL. (2003). Polymorphisms in candidate genes for type 2 diabetes mellitus in a Mexican population with metabolic syndrome findings. Diabetes Res. and Clinical Practice, 63:47-55.
7. Calderón Garcidueñas, A.N., Ruiz Flores, P., Cerda Flores, R.M., Barrera-Saldaña, Rojas Martínez, A. (2005) Clinical follow up of Mexican woman with early onset of breast cancer and mutations in the BRCA1 and BRCA2 genes. SaludPública de México vol.47, n° 2, marzo-abril.