Doctora Yolanda Villaseñor Navarro
El uso de la mamografía como método de detección temprana de cáncer mamario conduce al descubrimiento de lesiones clínicamente no palpables, algunas de ellas sospechosas para cáncer, por lo que se hace indispensable la corroboración histológica de las mismas.
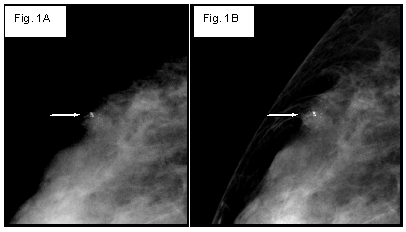
La mamografía de tamizaje se puede realizar en equipos análogos o digitales (Figura 1), ambos útiles en la detección temprana de cáncer de mama. La mamografía digital ha demostrado superioridad en la detección de lesiones mamarias en la mujer con mama densa (predominio de tejido glandular)1.
De acuerdo a lo señalado por la Norma Oficial Mexicana NOM-041-SSA2-20112, debe realizarse en mujeres sanas a partir de los 40 años, cada dos años; en mujeres sanas, con factores de riesgo para cáncer, debe realizarse 10 años antes del diagnóstico del familiar más joven.
Figuras 1 A y B. Mujer de 43 años, asintomática. Mamografía de tamizaje, magnificación, proyección cráneo caudal, con sistema análogo (Figura 1A) y digital (Figura 1B). Mama predominantemente glandular, con imagen nodular en cuadrante externo, parcialmente definido, de un centímetro aproximadamente y bordes oscurecidos (flecha larga). Asociada a calcificaciones puntiformes agrupadas (flecha corta). Reporte histopatológico: Carcinoma canalicular infiltrante.
Desde hace algunos años, los resultados de la mamografía se reportan en el sistema BI-RADS (Breast Imaging Reporting and Data System (sistema de reporte y de datos) el cual es útil para mantener una forma estandarizada de comunicar los resultados de una mamografía, y permite que los médicos utilicen las mismas palabras y se emitan recomendaciones3. Este sistema también se utiliza en imágenes mamarias por ultrasonido y resonancia magnética.
CATEGORÍAS BI-RADS
Categoría 0: requiere realizar estudios por imágenes adicionales o comparar con mamografías anteriores.
Categoría 1: hallazgo negativo.
Categoría 2: hallazgo benigno.
Categoría 3: hallazgo posiblemente benigno con seguimiento a corto plazo.Los hallazgos en esta categoría tienen una muy buena posibilidad (más de 98 por ciento) de ser benignos. Se realiza seguimiento a los seis meses, por dos años o hasta que se determine que el hallazgo está estable. Este enfoque evita biopsias innecesarias; pero si el área cambia a lo largo del tiempo, permite hacer un diagnóstico en sus inicios.
Categoría 4: anormalidad sospechosa, se debe considerar una biopsia.Los hallazgos sugieren la posibilidad de cáncer; tienen un rango amplio de niveles de sospecha. Por este motivo, algunos médicos pueden dividir esta categoría aún más:
- 4A: hallazgo con una sospecha baja de que sea cáncer
- 4B: hallazgo con una sospecha mediana de que sea cáncer
- 4C: hallazgo de preocupación moderada de que sea cáncer, pero no tan alta como la Categoría 5.
Categoría 5: anormalidad que sugiere firmemente que se trata de un hallazgo maligno; se deben tomar las acciones adecuadas. Los hallazgos tienen alta sospecha de cáncer y la probabilidad también es alta (95 por ciento) de que se corrobore cáncer. Se recomienda biopsia.
Categoría 6: resultados de biopsia conocidos con malignidad demostrada; se deben tomar las acciones adecuadas.
LA BIOPSIA, LO INDICADO
Posteriormente a una mamografía de tamizaje en mujer asintomática o ante una mujer con síntomas, en quienes se sospeche la presencia de una neoplasia maligna, deberá indicarse la realización de biopsia. Hasta hace algunos años, la biopsia escisional, previo marcaje con aguja percutánea, era la única herramienta de diagnóstico con exactitud en lesiones clínicamente ocultas de la mama.
En la actualidad, la biopsia no quirúrgica de lesiones no palpables de la mama, con agujas de corte, se ha convertido en una alternativa para evitar la cirugía4 y ha ayudado a reducir el número de biopsias quirúrgicas, además de emplear los quirófanos para manejo terapéutico y no diagnóstico. Por otra parte, la biopsia por aspiración con aguja fina para estudio citológico es útil en lesiones palpables, no así en lesiones no palpables en donde existe un alto reporte de muestras insuficientes. Es un estudio operador dependiente en la toma y lectura de la muestra, por lo que con las herramientas actuales para biopsia histológica con agujas de corte y corte aspiración, se prefieren en la mayoría de los centros en donde se realiza biopsia5.
La citología se emplea todavía en la evaluación de quistes mamarios, y es una herramienta fundamental en la evaluación de ganglios axilares, cuando existe sospecha de neoplasia primaria o metastásica en este nivel6.
Figura 2. Ultrasonido de región axilar derecha, en mujer con diagnóstico de cáncer de mama izquierda, etapa clínica ECIIIA. Se delimita ganglio con pérdida en su morfología y evidencia de cortical engrosada, y pérdida de hilio graso. Datos de sospecha para metástasis, se realiza biopsia aspiración con aguja fina (flecha).
En la actualidad, las biopsias percutáneas se realizan con diferentes métodos de guía por imagen, y esto depende directamente del método por el cual se visualiza la lesión mamaria:
Nódulo: denso, de bordes imprecisos con retracción de la piel o edema cutáneo
Figuras 3 A, B, C y D. Mujer 63 de años. Mamografía de tamizaje. Proyección Cráneo Caudal (Figura 3A) y Proyección Medio Lateral Oblicua (Figura 3B). Identifica nódulo de densidad media con bordes oscurecidos (Figura 3C Magnificación electrónica). Se realiza ultrasonido (Figura 3D), y se corrobora nódulo macrolobulado sólido con áreas quísticas en su interior. Se realiza biopsia con aguja de corte y guía sonográfico. Resultado histopatológico: carcinoma in situ de bajo grado, sin necrosis, con focos de invasión.
Micro calcificaciones agrupadas en un área pequeña, pleomorfas y de densidad variable
Figuras 4 A y B. Femenina, de 40 años, con masa palpable en mama derecha en cuadrante inferior interno. Secreción de pezón derecho de 8 meses de evolución. Las proyecciones mamográficas cráneo caudal (Figura 4A) y proyecciones Medio Lateral Oblicuas (Figura 4B) muestran acumulación de calcificaciones asociadas a distorsión de la arquitectura y presencia de ganglios axilares de apariencia metastásica (flecha). Diagnóstico histopatológico: carcinoma canalicular infiltrante, con extenso componente ductal y áreas de necrosis.
Zonas de distorsión de la arquitectura e incluso áreas de asimetría en densidad.
Figuras 5 A, B y C. Femenina, de 58 años, con área de induración en mama izquierda CII, enrojecimiento de la piel y retracción de pezón. Mamografía (Figuras 5A y B) con zona de densidad asimétrica, asociada a distorsión de la arquitectura en mama izquierda. En ultrasonido (Figura 5C) se demuestra un área hipoecoica extensa irregular, mal definida, con franca atenuación sónica posterior. Diagnóstico histo-patológico: carcinoma lobulillar.
La biopsia percutánea de lesiones mamarias guiadas por imagen tiene como indicación aquellas no palpables o clínicamente ocultas, aun y cuando actualmente se prefiere la biopsia guiada de lesiones palpables, ya que disminuye los falsos negativos en la toma de las mismas.
El método de imagen por el cual se guiará la biopsia dependerá del tipo de lesión detectada:
- Estereotaxia, para microcalcificaciones/distorsiones.
- Ultrasonido, para guía de biopsia de nódulos.
- En mujeres de riesgo elevado para cáncer de mama, la resonancia magnética aunada a la mamografía y el ultrasonido, puede detectar un mayor número de lesiones no vistas por los otros dos métodos, y la biopsia debe guiarse por RM. Más recientemente, la introducción del PEM (mamografía por emisión de positrones) para la evaluación, etapificación y seguimiento del cáncer de mama, puede detectar lesiones ocultas solo observadas por este método, por lo que al igual que la RM, ésta deberá realizarse con esta guía.
En algunos casos particulares, donde la sospecha de cáncer de mama es igual o mayor a 95 por ciento (BI-RADS Categoría 5) el tipo de biopsia que debe realizarse es controversial, y depende directamente de protocolos de tratamiento en cada centro. Se tienen como alternativas para la corroboración histológica, el marcaje percutáneo con aguja y la escisión quirúrgica de la lesión, con reporte histológico transoperatorio (cuando no se trata de microcalcificaciones); la decisión terapéutica se realiza en el mismo acto quirúrgico o en una segunda cirugía, en espera del resultado histológico definitivo. Otra alternativa es la biopsia percutánea con aguja de corte, y cuando el resultado es un carcinoma, se planea el tratamiento y se abaten costos, empleando los quirófanos para manejo terapéutico y no diagnóstico.
Lee CH, en su estudio, reporta que las lesiones sometidas a biopsia percutánea, y la Categoría 5, muestran menor costo en comparación con la biopsia quirúrgica7, 8.
LOCALIZACIÓN PERCUTÁNEA PREOPERATORIA
La localización preoperatoria se utiliza en el marcaje de las lesiones no palpables, detectadas por mamografía o en otros estudios de imagen (ultrasonido, resonancia magnética). El estudio se realiza en un equipo de mamografía y se efectúa compresión sobre la mama con una rejilla fenestrada graduada; se debe elegir el sitio de marcaje, considerando la localización de la lesión, tamaño de mama y abordaje quirúrgico.
La paciente requiere permanecer comprimida frente al equipo de mamografía unos minutos, mientras se realiza la asepsia y aplicación de anestésico local; se introduce el material seleccionado para el marcaje, el cual consiste en colorantes (azul de metileno, carbono, isótopos marcados9), agujas rígidas y combinación de agujas con arpón (todas ellas de diferentes longitudes y grosores), y se realizan proyecciones mamográficas para la ubicación del instrumento seleccionado. Los arpones y agujas se clasifican en reposicionables o fijos. Estos últimos, una vez liberados de la camisa, sólo es posible retirarlos en el quirófano, durante la escisión de la lesión.
Este procedimiento es perfectamente tolerado por las pacientes, pero debemos considerar que los tiempos son importantes, ya que, a medida del tiempo de compresión, la paciente puede presentar reflejos vaso vágales, lo que complica el procedimiento .
Una vez colocado el dispositivo, la paciente es llevada al quirófano, en donde se escindirá (cortará) la lesión. Para corroborar esto, la pieza escindida requiere ser radiografiada para la corroboración del procedimiento y la ubicación de la lesión con respecto a los bordes (¿fue escindida en su totalidad?, ¿se encuentra cercana o no a los bordes quirúrgicos?).
Figuras 6 A, B, C y D. Femenina, de 43 años, asintomática. En mamografía de detección: nódulo mal definido retro glandular en mama derecha. 6A). Rejilla fenestrada con colocación de aguja rígida tipo Hawkins, 6B). Proyección mamográfica CC, con colocación de aguja el centro de la lesión (6C y 6D). Pieza quirúrgica y radiografía de corroboración en donde se observa escisión completa de la lesión. Diagnóstico histológico: carcinoma canalicular infiltrante con SBR de 6.
COMPLICACIONES DEL PROCEDIMIENTO
El marcaje preoperatorio es un proceso relativamente simple, con complicaciones poco frecuentes, tales como sangrado, infección, reacciones vasovagales, fallas en la escisión de la lesión, migración de los arpones.
BIOPSIA POR ULTRASOSNIDO
La biopsia guiada por ultrasonido es útil, tanto como guía para colocación de arpones, como en las biopsias con aguja de corte. El procedimiento se realiza con la paciente en decúbito supino, asepsia de la zona y aplicación de anestésico local; se localiza la lesión y se visualiza la toma de biopsia en tiempo real10.
Figuras 7 A, B, C y D. Femenina, de 51 años. Mamografía diagnóstica, lesión espiculada en cuadrante superior de la mama derecha (Figura 7A). El ultrasonido en mama derecha (Figura 7B) delimita lesión hipoecoica de borde espiculado en radio 12 línea B, atenuación sónica posterior y de paredes irregulares. Se realiza biopsia guiada por ultrasonido con pistola automática y aguja de corte (Figuras 7 C y D). Diagnóstico histológico: carcinoma canalicular infiltrante SBR 7.
Las biopsias guiadas por ultrasonido y aguja de corte son confiables en cuanto a precisión. Estadísticamente, el reporte de falsos negativos es de 3-9 por ciento, con una sensibilidad de 96.3 por ciento. La correlación de los hallazgos radiológicos y patológicos, y el seguimiento en resultados benignos, son esenciales en el éxito de las biopsias de este tipo11.
La biopsia con aguja de corte y guía sonográfica es una herramienta invaluable en el diagnóstico de las lesiones mamarias vistas por este método, lo que queda básicamente restringido a los nódulos, aun y cuando es factible realizar biopsia guiada por este método en microcalcificaciones agrupadas, cuando sean observadas por ultrasonido12.
Ventajas de la biopsia guiada por ultrasonido sobre estereotaxia: Visualización en tiempo real de la aguja, no uso de radiación ionizante ni compresión de la mama, confort del paciente, muestra multidireccional con accesibilidad a cualquier área de la mama o axila, bajo costo13.
BIOPSIA GUIADA POR ESTEREOTAXIA
El principio de la estereotaxia se basa en la localización exacta de una lesión en tres dimensiones, pudiendo determinarse por el cambio de posición de la lesión respecto a dos imágenes (estereotaxia)14.
La biopsia percutánea guiada por estereotaxia está indicada en:
- Lesiones no vistas por ultrasonido.
- Asimetría y distorsiones de la arquitectura.
- Principalmente en calcificaciones.
Las biopsias guiadas por estereotaxia, empleando agujas de corte y pistola automática o herramientas con corte aspiración, son muy útiles y de mínima invasión, y constituyen una evidente alternativa para la biopsia quirúrgica, ya que los errores diagnósticos son comparables con los obtenidos en biopsias quirúrgicas. Se estima que los errores de biopsias quirúrgicas son menores al 2 por ciento14, 15.
Los resultados histológicos de hiperplasia ductal atípica o carcinoma in situ, deben ser llevados a biopsia escisional, ya que la subestimación de lesiones in situ e infiltrantes es muy importante (20 por ciento de pacientes con diagnóstico de ductal in situ se convierten en infiltrantes en biopsia escisional). Los reportes de neoplasia lobular in situ se consideran marcadores de riesgo, por lo que no requieren escisión. Cuando existe la sospecha radiológica de cicatriz radial, la biopsia escisional es la indicada, ya que es difícil para el patólogo diferenciarla de carcinomas tubulares, o durante la biopsia omitir una lesión maligna adyacente16.
Cuando la biopsia se ha debido a microcalcificaciones, es indispensable realizar radiografías de las muestras, para asegurarse que estas serán estudiadas.
Se requiere, en primer lugar, de equipos de mamografía con aditamento para estereotaxia. En el mercado existen diferentes manufacturas y básicamente dos sistemas: equipos verticales y mesa prono (Figura 8), cada una de ellas con ventajas y desventajas.
Existe la posibilidad de unidades digitales para estereotaxia, lo que agiliza el procedimiento. Las biopsias guiadas por estereotaxia se realizan con agujas de corte y pistola automática. Para los marcajes percutáneos para biopsia escisional,se prefiere localización con rejillas fenestradas.
Figuras 8 A, B, C y D. Equipo de estereotaxia. Bipedestación (Figura 8A). Estereotaxia prono (Figura 8B). Proyección de localización de calcificaciones en equipo de estereotaxia, pre biopsia (Figura 8C). Toma de muestra de biopsia guiada por estereotaxia con equipo de corte aspiración (Figura 8D).
Complicaciones en la biopsia por estereotaxia:
- Incapacidad de realizar el procedimiento por una valoración previa inadecuada.
- Sangrado.
- Infección.
- Hematoma.
- Reflejos vaso vagales (en equipos verticales).
La localización de lesiones no palpables de la mama guiada por imagen, se convierte en una herramienta básica en el diagnóstico de lesiones no palpables de la mama. Recientemente se ha demostrado su utilidad en biopsias de lesiones palpables.
La Resonancia Magnética puede detectar cáncer en etapa temprana, en especial en mujeres con mama densa y/o mujeres de alto riesgo para cáncer de mama. Ésta cuenta con indicaciones muy específicas; además de las ya mencionadas, es útil en mujeres con implantes, así como en mujeres con diagnóstico de cáncer de mama para etapificación y seguimiento.
En las mujeres en quienes se realiza resonancia magnética, con mamografía y ultrasonido negativos, y resonancia con hallazgos de sospecha, la RM puede ser el método guía de una biopsia 17.
REFERENCIAS
- Hubbard RA, Zhu W, Horblyuk R, Karliner L, Sprague BL, Henderson L, Lee D, Onega T, Buist DS, Sweet A. Diagnosticimaging and biopsypathwaysfollowingabnormalscreen-film and digital screeningmammography.BreastCancer Res Treat. 2013 Mar 8.
- Norma Oficial Mexicana NOM-041-SSA2-2011, Para la prevención, diagnóstico, tratamiento, control y vigilancia epidemiológica del cáncer de mama, la mamografía.
- D’Orsi CJ, Bassett LW, Berg WA, et al. BI-RADS: Mammography, 4th edition in: D’Orsi CJ, Mendelson EB, Ikeda DM, et al: Breast Imaging Reporting and Data System: ACR BI-RADS – Breast Imaging Atlas, Reston, VA, American College of Radiology, 2003
- Bruening W, Fontanarosa J, Tipton K, Treadwell JR, Launders J, SchoellesK.SourceSystematicreview: comparativeeffectiveness of core-needle and open surgicalbiopsytodiagnosebreastlesions. Ann InternMed. 2010 Feb 16;152(4):238-46.
- O’Flynn EA, Wilson AR, Michell MJ. Image-guided breast biopsy: state-of-the-art.ClinRadiol. 2010 Apr; 65(4):259-70.
- Oz A, Demirkazik FB, Akpinar MG, Soygur I, Baykal A, Onder SC, Uner A. Efficiency of ultrasound and ultrasound-guided fine needle aspiration cytology in preoperative assessment of axillary lymph node metastases in breast cancer. J Breast Cancer. 2012 Jun;15(2):211-7. doi: 10.4048/jbc.2012.15.2.211.
- Shetty MK. Presurgicallocalization of breastabnormalities: anoverview and analysis of 202 cases.Indian J SurgOncol.2010 Dec;1(4):278-83.
- Lieu D. Breast imaging for interventional pathologists.Arch Pathol Lab Med.2013 Jan;137(1):100-19.
- Van Esser S, Hobbelink M, Van der Ploeg IM, Mali WP, Van Diest PJ, BorelRinkes IH, Van Hillegersberg R. Radio guidedoccult lesion localization (ROLL) for non-palpable invasive breast cancer. J SurgOncol. 2008 Dec 1;98(7):526-9. doi: 10.1002/jso.21143
- Wiratkapun C1, MD, Treesit T1, MD, Wibulpolprasert B1, MD, Lertsithichai P2, MD, MScDiagnosticaccuracy of ultrasonography-guidedcoreneedlebiopsyforbreastlesionsSingaporeMed J 2012; 53(1) : 40.
- Ricci MD, Calvano Filho CM, Oliveira Filho HR, Filassi JR, Pinotti JA, Baracat EC. Analysis of the concordance rates between core needle biopsy and surgical excision in patients with breast cancer. Rev Assoc Med Bras. 2012 Oct;58(5):532-6.
- Zheng J, Alsaadi T, Blaichman J, Xie X, Omeroglu A, Meterissian S, Mesurolle B. Invasive ductal carcinoma of the breast: correlation between tumor grade determined by ultrasound-guided core biopsy and surgical pathology.AJR Am J Roentgenol. 2013 Jan; 200 (1).
- Apesteguía L, Pina LJ. Ultrasound-guided core-needle biopsy of breast lesions Insights Imaging. 2011 August; 2(4): 493–500.
- Victoria Ames & Peter D. BrittonStereotacticallyguidedbreastbiopsy: a reviewInsightsImaging (2011) 2:171–176 DOI 10.1007/s13244-010-0064- Published online: 20 January 2011 # EuropeanSociety of Radiology 2011.
- Ji Hyun Youk, MD, Eun-Kyung Kim, MD, […], and HaeYoun Kang, MD Concordant or Discordant? Imaging-Pathology Correlation in a Sonography-Guided Core Needle Biopsy of a Breast Lesion Korean J Radiol 2011;12(2):232-240.
- Ferris M. Hall, MD Identification, Biopsy, and Treatment of PoorlyUnderstoodPremalignant, in Situ, and IndolentLow-Grade Cancers: Are WeBecomingVictims of OurOwnSuccess? Radiology 2010; 254:655–659.
- Frank Fischnach, Holm Eggemann, Juergen Bunke, Uta Wonneber, Jens Ricke and Katharina Strach. MR-guided Freehand Biopsy of Breast Lesions in a 1.0-T Open MR Imager with a Near-Real-time Interactive Platform: Preliminary Experience Radiology November 2012 265:2 359–370.