POR ANDREW MYERS
Traducido por Alejandro Ramos de la Peña
 Oscar Abilez y un equipo multidisciplinario de especialistas desarrollaron las primeras células de corazón humano que pueden contraerse en respuesta a determinados tipos de luz.
Oscar Abilez y un equipo multidisciplinario de especialistas desarrollaron las primeras células de corazón humano que pueden contraerse en respuesta a determinados tipos de luz.
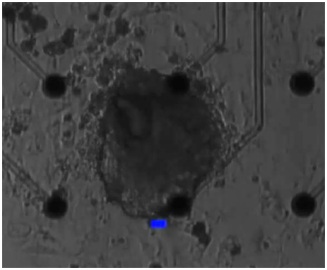
En un espacio compacto de un laboratorio de la Universidad de Stanford, Oscar Abilez, MD, analiza en un microscopio una pequeña colección de células en una caja de Petri. Una grabadora de video proyecta lo que el microscopio ve en un monitor cercano. Las células en la caja de petri pulsan rítmicamente, una vez por segundo. Las células son los cardiomiocitos, encargados de generar la contracción cardiaca y la función de marcapasos del corazón humano.
Abilez levanta un dedo como si fuera a decir: «Espera», y alcanza una pequeña palanca oculta detrás del microscopio. Con el mismo dedo, mueve de un tirón la palanca hacia arriba. Una luz azul pálida, inunda la caja de petri. Abilez apaga la luz y luego la enciende, rápido y luego lento. Cada vez que el dedo se eleva, las células cardiacas se contraen de acuerdo con la luz.
En un artículo publicado el 21 de septiembre en el Biophysical Journal, Abilez, autor principal del artículo e investigador postdoctoral y estudiante de doctorado en bioingeniería, y un equipo multidisciplinario de Stanford describen la forma en que lograron, por primera vez, la inducción del ritmo de contracción en células del corazón humano mediante luz, utilizando una tecnología llamada optogenética.
En el corto plazo, dicen los investigadores, el avance proporcionará nuevos conocimientos sobre la función del corazón. A largo plazo, sin embargo, el desarrollo podría conducir a marcapasos basados en luz y parches de tejido genéticamente modificados para ser compatibles para reemplazar el músculo dañado por un infarto al corazón.
Actualmente, los marcapasos eléctricos implantados quirúrgicamente y los desfibriladores son la norma, regulando el pulso de contracción de millones de corazones en todo el mundo. “Pero esto no está libre de problemas,” comenta Abilez. “Los marcapasos fallan mecánicamente. Los electrodos pueden causar daños en los tejidos.”
“Nosotros podríamos, por ejemplo, crear un marcapaso que no estuviera en contacto físico con el corazón,” dijo Christhoper Zarins, MD, coautor y profesor emérito de cirugía y director del laboratorio donde Abilez llevó a cabo sus experimentos. “En vez de implantar quirúrgicamente un dispositivo que tiene los electrodos dentro del corazón, nosotros inyectaríamos estas células sensibles a la luz en el corazón dañado y se establecería el pulso de manera remota con luz, posiblemente fuera del corazón.”
Para crear las células cardiacas con capacidad de respuesta a la luz, los investigadores primero insertaron el ADN que codifica una proteína sensible a la luz llamada canalrodopsina-2, o ChR2, en células madre embrionarias humanas. La ChR2 controla el flujo de iones con carga eléctrica en la célula. Para las células del corazón, el principal ión es el sodio, que inicia una cascada electroquímica que hace que la célula se contraiga. Después transforman a las células madre modificada con ingeniería optogenética en cardiomiocitos los cuales, a diferencia de otros, son capaces de responder a la luz.
La proteína de mayor importancia para el experimento es la ChR2, que es sensible a una longitud de onda muy específica de la luz azul y regula pequeños canales en la superficie celular. Cuando la ChR2 es iluminada por la longitud de onda correcta de luz azul, los canales se abren para permitir un flujo de iones de sodio cargados eléctricamente en el interior de la célula, produciendo una contracción.
Texto obtenido de:
http://med.stanford.edu/ism/2011/september/cardiomyocyte.html
Imagen obtenida de: