Doctor en Medicina
Dionicio Ángel Galarza Delgado
Jefe del Departamento de Medicina Interna Hospital Universitario
Doctora María del Carmen Velarde Ochoa
Residente de Reumatología e Inmunología Clínica Hospital Universitario
medint@hospitaluniversitario.org
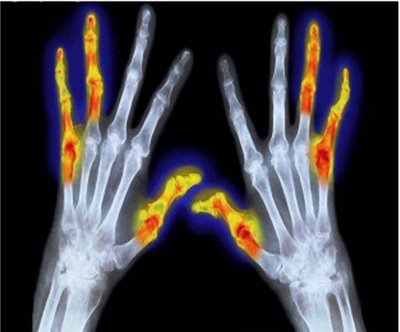
 La artritis reumatoide (AR) es una enfermedad sistémica, autoinmune e inflamatoria crónica, caracterizada por la inflamación y destrucción del cartílago articular, en asociación con evidencia serológica de auto-reactividad; su prevalencia es de 0.3 por ciento y afecta a mujeres 2.5 veces más que a hombres, entre la cuarta y quinta década de la vida.
La artritis reumatoide (AR) es una enfermedad sistémica, autoinmune e inflamatoria crónica, caracterizada por la inflamación y destrucción del cartílago articular, en asociación con evidencia serológica de auto-reactividad; su prevalencia es de 0.3 por ciento y afecta a mujeres 2.5 veces más que a hombres, entre la cuarta y quinta década de la vida.
Durante mucho tiempo se tuvo la noción de que la AR era un problema relativamente menor, puesto que causaba dolor articular y rigidez, pero que no tenía las consecuencias de padecimientos de mayor impacto, como la diabetes mellitus o el cáncer. Actualmente, sabemos que este enfoque era erróneo, puesto que las personas con AR tienen una esperanza de vida de 10 a 18 años menos que la población general, con cifras de mortalidad semejantes a las de los pacientes con enfermedad coronaria de tres vasos y linfoma de Hodking.
Dicho de otra manera, este padecimiento implica no solamente menor calidad de vida, sino también, y destacadamente, menos tiempo de vida, y, lo que es peor, una reducción de los años de vida saludables.
DEVASTADOR IMPACTO ECONÓMICO
Además, el impacto económico de esta enfermedad, puede ser devastador, derivado de los costos directos relacionados con su atención, llámense consultas médicas, exámenes de laboratorio y compra de medicamentos, junto con los costos indirectos, resultado de la pérdida de la capacidad laboral, en un grupo de edad habitualmente muy productivo, sin hacer menos los costos intangibles relacionados con la ansiedad y la depresión asociados a la enfermedad.
Por lo antedicho, en la actualidad, y sobre todo en los países del primer mundo, a las enfermedades reumáticas en general, y a la AR en particular, se les brinda una importancia especial, con un enfoque primario orientado a su detección oportuna y al tratamiento temprano, a través de múltiples estrategias, encabezadas por la educación y un cambio de paradigma cultural entre los médicos y los diferentes actores sociales.
De hecho, algunos autores consideran la AR como una verdadera emergencia de salud, que requiere una actitud terapéutica activa de parte de los médicos, para su pronta identificación e implementación de un manejo apropiado.
Los objetivos actuales del tratamiento en Artritis Reumatoide son:
1) Reducir o eliminar el dolor articular e inflamación, prevenir el daño articular, minimizar la discapacidad y mantener el empleo.
2) Tratar de alcanzar la remisión o baja actividad de la enfermedad tan pronto sea posible, en cada paciente, en un lapso de tres a seis meses.
FÁRMACOS ANTI-REUMÁTICOS
Con el fin de alcanzar estos objetivos, el tratamiento con fármacos anti-reumáticos modificadores de la enfermedad (FARMES), debe ser iniciado tan pronto se realice el diagnóstico de artritis reumatoide.
En las últimas décadas, se han logrado avances importantes en el entendimiento de los mecanismos de producción de esta enfermedad, principalmente en el área de la inmunología y la biología molecular, así como el rol clave de los factores genéticos para su inicio y desarrollo, lo que permite un manejo más racional, orientado a evitar las deformidades irreversibles que pueden presentarse como complicaciones graves en estos pacientes.
En ese mismo sentido, una corriente moderna de atención integral de los pacientes con AR consiste en personalizar al máximo los tratamientos, considerando no sólo los factores clínicos y de laboratorio tradicionales, sino expandiendo este campo con la introducción de biomarcadores específicos, tanto genéticos como clínicos y paraclínicos, que dan la pauta para el diseño de una estrategia terapéutica individualizada, que a su vez facilita el logro de los objetivos terapéuticos antes mencionados.
En los últimos 50 años, el desarrollo de nuevas terapias con FARMES ha revolucionado el tratamiento de la AR. Inicialmente, en 1920, la base del tratamiento era monoterapia; posteriormente, en 1960, se introdujo el concepto de pirámide terapéutica, en que el tratamiento inicial se basaba en el uso de anti-inflamatorios no esteroideos, reposo y educación del paciente, seguido por escalamiento hacia terapias más potentes, sólo si había destrucción articular demostrada radiográficamente, lo cual tenía como gran inconveniente la progresión de la enfermedad en la gran mayoría de los pacientes, quienes terminaban severamente discapacitados.
VENTANA DE OPORTUNIDAD
A principios de 1990, se dio a conocer la hipótesis de “ventana de oportunidad”, referida al período de tiempo -al principio de la enfermedad- durante el cual es posible conseguir una respuesta terapéutica importante, que originaría una mejoría a largo plazo o incluso la remisión indefinida de la enfermedad.
Esta hipótesis ha sido confirmada por diversos estudios reportados en la literatura internacional, entre ellos FIN-RACO (estudio finlandés) y COBRA (estudio holandés de terapia combinada), los cuales demostraron que el retraso en el inicio del tratamiento predice una menor posibilidad de remisión en los pacientes con monoterapia, y que el 70-90 por ciento de los pacientes sufren daño radiográfico en los primeros dos a tres años del inicio del padecimiento.
En estas condiciones, en 1994 se introdujo el término de intervención temprana; en 1999, el de terapia combinada, y en el año 2000, el mejor entendimiento de la patogénesis molecular de la AR permitió el desarrollo de la terapia biológica, dirigida contra componentes específicos de la respuesta inmune.
MANEJO PERSONALIZADO
El alto costo de estos tratamientos hace imperativo un manejo personalizado, que disminuya los periodos de actividad de la enfermedad y la exposición innecesaria a efectos colaterales adversos indeseables que pueden ocasionar estos medicamentos.
El arsenal terapéutico actual para la AR está constituido por diversos fármacos, como son: anti-inflamatorios no esteroideos (AINES), glucocorticoides, FARMES clásicos y FARMES biológicos.
Los AINES son utilizados principalmente como tratamiento sintomático por sus efectos analgésicos y anti-inflamatorios; sin embargo, no detienen la progresión de la enfermedad, por lo que, aunque necesarios, nunca serán suficientes para tratar a una persona con AR.
Con respecto a los glucocorticoides, su uso por primera vez para el tratamiento de pacientes con AR, en la Clínica Mayo, en Rochester, Minnesota, le valió a Philip S. Hench ganar el Premio Nobel de medicina en 1950.
Estos medicamentos son los anti-inflamatorios más potentes disponibles, y, por tanto, de gran valía en el manejo de estos casos, aunque su gran toxicidad potencial obliga a que su uso deba ser muy racional.
LOS FARMES
Los FARMES clásicos (químicos), son un grupo diverso de agentes terapéuticos que reducen los signos y síntomas de la AR y retrasan la progresión radiográfica del daño articular; esta clase de medicamentos son esenciales en el control de la AR y deben estar en el tratamiento de todos los pacientes, e incluyen: Metotrexate, Sulfasalazina, Leflunomida, Hidroxicloroquina, Cloroquina, Azatioprina, Ciclosporina A, Ciclofosfamida, D-penicilamina y Sales de oro.
Los FARMES biológicos son medicamentos obtenidos de organismos vivos; en su gran mayoría son proteínas, producidas a través de procesos biotecnológicos; es decir, tecnología basada en la biología (biotecnología). Muchas de éstas son moléculas producidas para bloquear citocinas proinflamatorias, que juegan un papel fundamental en la patogénesis de la AR; en general, los biológicos son considerados FARMES, porque han demostrado disminuir la progresión del daño articular, e incluyen inhibidores del Factor de necrosis tumoral (anti-TNF), los cuales son: Etanercept (Proteína de fusión soluble del receptor del TNF p75), Infliximab (anticuerpo monoclonal quimérico) y Adalimumab (anticuerpo monoclonal humanizado).
También tenemos Anakinra (Antagonista del receptor de la interleucina 1); Tocilizumab (anticuerpo monoclonal humanizado, dirigido contra el receptor, tanto soluble como de membrana, de la interleucina-6 (IL-6); Rituximab (anticuerpo monoclonal quimérico contra CD20), y Abatacept (inhibidor de la coestimulación CD28).
OPCIONES TERAPÉUTICAS MÚLTIPLES
Como puede verse, el número de opciones terapéuticas para el tratamiento de la AR es grande, y además creciente, por lo que se significan como una gran esperanza y oportunidad para los pacientes. Sin embargo, esta misma diversidad tiene como cara opuesta la dificultad para realizar la mejor selección para un paciente en lo particular, hecho que aún es más relevante cuando sabemos que la historia natural de la AR es variable, y que lo mismo hay casos de enfermedad leve en un extremo, así como casos catastróficos en el otro, y que en un principio puede en ocasiones ser difícil predecir el curso que tendrá tal o cual paciente.
Es aquí donde los conocimientos recientes en áreas como la farmacogenética resultan de gran utilidad para la toma de decisiones en la práctica cotidiana. Hoy en día, sabemos que existen determinantes genéticos (HLA-DRB1, PTPN22, enzimas citocromo p450); factores de la enfermedad (duración de la enfermedad, actividad de la enfermedad, reactantes de fase aguda, autoanticuerpos); factores del huésped (edad, género, comorbilidades, uso previo de FARMES), y factores del medio ambiente (dieta, tabaquismo) que juegan un papel importante en la variación de la respuesta al tratamiento.
PREDICTORES DE RESPUESTA A FÁRMACOS MODIFICADORES
Desde principios de 1980, el metotrexate ha sido el tratamiento de primera línea, por su perfil de seguridad, sus propiedades modificadoras de la enfermedad y su habilidad para potenciar los efectos de otras terapias farmacológicas. En el ámbito celular, el metotrexate inhibe las enzimas de la vía de los folatos, incluidos dihidrofolato reductasa (DHFR), timidilato sintetasa (TYMS) y la 5-aminoimidazol-4-carboxamida ribonucleótido (ATIC); además, influyen indirectamente en la enzima metilentetrahidrofolato reductasa (MTHFR).
Una extensa revisión de la farmacogenética del metotrexate muestra la evidencia de varios polimorfismos en los genes codificadores de dichas enzimas, relacionados con la eficacia y seguridad del metotrexate.
Los polimorfismos que han sido relacionados con incremento en la respuesta a metotrexate son: polimorfismo G80A del gen RFC1, C3435T del gen ABCB1, A1298C del gen MTHFR y deleción del 3/UTR 6pb del gen TYMS; sus efectos son incremento en la entrada de MTX dentro de la célula, disminución en la actividad de MTHFR y disminución en la estabilidad y expresión de RNA mensajero.
Los polimorfismos asociados con disminución de la eficacia del metotrexate son repetición del 5/UTR 28pb del gen TYMS, lo que provoca un incremento en la expresión de RNA mensajero y en la actividad de enzimas; y el que se asocia con un incremento en los efectos adversos gastrointestinales y un incremento en la toxicidad hepática es el C677T del gen MTHFR.
La azatioprina es otro fármaco modificador de la enfermedad, utilizado en el tratamiento de la AR; su mecanismo de acción es disminuir la síntesis de novo de los nucleótidos de purina, disminuir la proliferación celular de linfocitos T y B, así como de monocitos y supresión de la actividad de las células Natural Killer.
La investigación en farmacogenética se ha centrado en la enzima tiopurina S-metiltransferasa (TPMT), y se ha documentado que los polimorfismos TPMT*2, TPMT*3A y TPMT*3C se relacionan con toxicidad hematológica y gastrointestinal, debido a actividad baja o intermedia de dicha enzima.
PREDICTORES DE RESPUESTA A INHIBIDORES DEL FACTOR DE NECROSIS TUMORAL
Algunos de los predictores clínicos de respuesta a anti-TNF son también considerados factores de mal pronóstico en AR, tales como altos niveles de actividad, sexo femenino, títulos altos de factor reumatoide (FR) y anticuerpos contra péptido cíclico citrulinado (anti-CCP), los cuales se asocian con menor probabilidad de alcanzar la remisión a un año.
Se han realizado estudios genéticos, en los cuales se han identificado polimorfismos de genes, asociados con la respuesta a inhibidores del factor de necrosis tumoral; entre ellos, el polimorfismo 308AA del gen del factor de necrosis tumoral ha sido implicado en falla de respuesta a los anti-TNF, mientras que el polimorfismo 808GG ha sido identificado en asociación con buena respuesta al tratamiento.
Un estudio reciente ha demostrado incremento en el biomarcador transcripcional CD11c, en respondedores a adalimumab, así como se han identificado perfiles transcripcionales asociados con la respuesta subsecuente a infliximab.
El registro de biológicos de la Sociedad Británica de Reumatología (BSRBR) sugiere que la ausencia de administración concomitante de AINES y metotrexate reduce la probabilidad de respuesta, principalmente del etanercept, y los fumadores son menos respondedores a infliximab. Además, los pacientes con altos niveles de proteína C reactiva tienen respuesta insuficiente a infliximab a dosis de 3mg/kg.
Respecto de los autoanticuerpos (FR, anti-CCP) como biomarcadores de respuesta al tratamiento, se ha identificado que pacientes seropositivos responden menos a inhibidores del factor de necrosis tumoral, o que la probabilidad de respuesta correlaciona inversamente con el título de autoanticuerpos.
PREDICTORES DE RESPUESTA A RITUXIMAB
Debido al papel de las células B en la patogénesis de la AR, en la producción de auto anticuerpos (FR y anti-CCP), presentación de antígeno y secreción de citocinas pro-inflamatorias, los estudios IMAGE y SERENE confirmaron la pérdida de eficacia del Rituximab en pacientes sero-negativos con AR temprana y en AR tardía, por lo que solamente debe ser considerado en pacientes seropositivos; así como niveles elevados de PCR están asociados con una mayor respuesta a rituximab.
Hasta el momento, no hay estudios que investiguen predictores genéticos de respuesta a rituximab en AR. Asimismo, no existen estudios que hayan investigado predictores genéticos o biomarcadores de respuesta al resto de los agentes biológicos.
CONCLUSIÓN
El tratamiento de la AR ha sido revolucionado en los últimos 20 años. El desarrollo de nuevas terapias biológicas permite inhibir citocinas proinflamatorias selectivamente, que nos permiten controlar la actividad de la enfermedad clínica y evitar la progresión radiológica.
Sin embargo, a pesar de estos nuevos agentes, el metotrexate continúa siendo el agente principal en el tratamiento de la AR debido a su eficacia, costo y seguridad, sin olvidar que el tratamiento debe ser individualizado en cada paciente, tomando en cuenta comorbilidades, factores de mal pronóstico, actividad y tiempo de evolución de la enfermedad, biomarcadores y marcadores genéticos.
Son necesarios estudios prospectivos de cohorte para tener datos más sólidos, así como estudios basados en los perfiles transcripcionales y biopsias sinoviales, que nos proporcionen una mayor evidencia de los factores predictores de respuesta al tratamiento, para mejorar el porcentaje de respuesta, preservar la estructura y función de las articulaciones, así como reducir los costos y mejorar la calidad de vida en estos pacientes.
Para tal efecto, una estrategia basada en la práctica de una medicina personalizada, que reconozca la tremenda variabilidad biológica de cada paciente, y que privilegie el uso de las herramientas clínicas, de los biomarcadores, de los factores genéticos y de los múltiples elementos que constituyen la riqueza del ser humano como un ente único e irrepetible, será la plataforma que nos permitirá el diseño de mejores esquemas aplicables a los pacientes con AR, no sólo en la esfera terapéutica, sino también en los ámbitos diagnóstico y pronóstico.