Doctor Hugo Alberto Barrera Saldaña
M. C. Carmen Yazmín Muñoz Mejía
M. C. Gregorio Antonio Alcázar González
M. C. Idalia Flores Argüello
Laboratorio de Bioanálisis
Genómicos de Vitagenésis S.A. de C.V.
El cáncer de colon es uno de los padecimientos que provoca mayor mortalidad en el mundo, ya que se estima que cobra cada año las vidas de cerca de 500 mil pacientes. En México, anualmente se diagnostican alrededor de once mil nuevos casos, y la tendencia revela que esta neoplasia va en aumento.
Este padecimiento comienza por un pólipo que, con el tiempo, se va transformando en un tejido canceroso, y su único tratamiento es la cirugía, seguida por quimioterapias desgastantes y dolorosas para el paciente.
Si bien la familia de los genes RAS ha estado implicada en la génesis de este tumor maligno durante más de 20 años, es hasta ahora cuando se dispone de datos convincentes que trasladan la información generada en la investigación a la práctica clínica.
BIOLOGÍA MOLECULAR
Se ha demostrado clínicamente que el gen K-ras, miembro de la referida familia RAS, desempeña un papel clave en la vía de señalización del receptor (R) del factor de crecimiento epidermal (EGF, por sus siglas en inglés). Tras su activación por el EGF, este receptor (EGFR) promueve la actividad de segundos mensajeros intracelulares que terminan activando la proteína KRAS, para determinar diferentes funciones que resultan en alteraciones en la expresión de genes reguladores de la proliferación y diferenciación celular, así como de la muerte celular programada o apoptosis.
Las mutaciones en el gen K-ras, se ubican mayoritariamente en los codones 12 y 13 de su segundo exón, y se presentan en un 30 a un 40 por ciento de los cánceres colorrectales. Las mutaciones resultan en la pérdida del control y por endeactivación de forma constitutiva de la proteína KRAS, provocando una señalización continua con independencia de si el propio EGFR se ha activado o inhibido terapéuticamente, estimulando independientemente de ello la proliferación tumoral.
Dichas mutaciones se han observado frecuentemente en el estadio tardío de un adenoma o etapa avanzada del cáncer, y su detección deviene en un biomarcador que representa un predictor negativo a la respuesta de la terapia anti-EGFR. El examen de rastreo de esta clase de mutaciones se considera una prueba de acompañamiento del tratamiento de esta neoplasia con biológicos dirigidos contra el EGFR.
Entre los primeros tratamientos para el cáncer colorrectal metastásico figura la administración de fármacos de naturaleza biológica, como los anticuerpos monoclonales: el cetuximab (Erbitux) y el panitumab (pmab), los cuales pretenden que la tasa de respuesta se incremente y el tiempo de supervivencia se prolongue, mediante el bloqueo del EGFR. Actualmente, la terapia de bloqueo de EGFR mediante Erbitux y demás fármacos monoclonales ha demostrado ser una buena opción para el cáncer colorrectal avanzado, ya que se ha observado que la tasa de respuesta mejora y el tiempo de metástasis/supervivencia se prolonga en los pacientes carentes de mutaciones en los codones 12 y 13, lo que no ocurre en aquellos pacientes cuyo gen Kras se encuentre mutado en estos codones.
Más recientemente, y gracias a los avances primero de la biología molecular y ahora de las ciencias genómicas, los análisis del genoma enfocados en este padecimiento buscan predecir no sólo la eficacia, sino también las reacciones adversas a los medicamentos, para sustentar terapias muy específicas e individualizadas, dando cauce a la denominada “medicina personalizada”, en la que, con base en la variación genómica de cada paciente, se prescribe un régimen medicamentoso.
FARMACOLOGÍA EN LA ERA GENÓMICA
Hoy en día, millones de pacientes alrededor del mundo han recibido un diagnóstico tardío o equivocado para alguna enfermedad, o alguna prescripción médica que, al no ser la más adecuada para la enfermedad de un paciente en particular, falla en detenerla e incluso si tampoco es la correcta, aunque funcione para la mayoría de los otros pacientes con padecimientos similares, a dicho paciente le provoca toxicidad o hasta la muerte.
Estas fallas diagnósticas y terapéuticas por falta de información de la variabilidad individualizada del genoma de cada paciente también se aplican al caso de las transfusiones sanguíneas y trasplantes de órganos.
Una gran cantidad de variaciones en el genoma puede influir en cada uno de estos casos. Por ello, las ciencias genómicas buscan convertir la valiosa información revelada por el recientemente concluido proyecto de secuenciación del genoma humano, tanto en nuevas pruebas diagnósticas (genética molecular), como en nuevas pruebas predictivas que definen riesgos personales de padecer enfermedades con componente genético (medicina genómica), así como para predecir el éxito de tratamientos farmacológicos (fármacogenómica).
Esto es posible gracias al advenimiento de los microarreglos o chips de ADN, que son por lo general laminillas de vidrio portadoras de miles de fragmentos de ADN sintéticos, que detectan, por hibridación, mutaciones, polimorfismos génicos y alteraciones en el número de copias de ciertas regiones del genoma.
Este nuevo enfoque de la medicina y sus innovaciones tecnológicas, hacen posible:
1. Predecir qué medicamentos y dosis de los mismos son la mejor opción para combatir las enfermedades de un determinado paciente, logrando con ello un mayor cuidado de su integridad física, al evitar la experimentación con medicamentos y dosis no prescritas con precisión.
2. Proteger la economía de los pacientes, al evitar estudios, consultas y medicamentos innecesarios para tratar sus enfermedades, a causa de diagnósticos equivocados.
3. Emitir a los médicos recomendaciones sobre las enfermedades predichas, en función del perfil genómico de cada paciente.
4. Permitir igualmente una gestión más eficiente de recursos hospitalarios y de médicos especialistas en el cuidado de la salud.
En estos casos, dicha información no sólo contribuirá a brindar oportunamente los mejores tratamientos, sino incluso a asesorar a las personas en riesgo y a sus familiares, para que adopten las mejores decisiones reproductivas, hábitos de vida y regímenes terapéuticos, con miras a minimizar los impactos de las enfermedades que la herencia les condiciona a padecer.
Estos nuevos dispositivos diagnósticos de la era genómica son verdaderas innovaciones de biotecnología genómica al servicio de los laboratorios de diagnóstico molecular.
FARMACOGENÓMICA EN CÁNCER DE COLON
El C-PHARMA es uno de los referidos dispositivos diagnósticos de la era genómica, diseñado para ayudar a los pacientes con cáncer de colon a conocer su predisposición metabólica a varios de los principales medicamentos disponibles para combatir su padecimiento, lo que permite elegir el tratamiento que les ofrezca la mejor eficacia y la menor toxicidad, en función de la particularidad de la variabilidad de su genoma.
Entre los medicamentos generalmente utilizados en los tratamientos quimioterapéuticos para el cáncer de colon y que pueden provocar toxicidad grave si existe deficiencia en las enzimas responsables para su catabolismo o eliminación, se encuentran el 5-FU, la capecitabina y el irinotecan, siendo los dos primeros asociados a un riesgo incrementado de toxicidad, debido a la deficiencia de la enzima DPD (Dihidropirimidina deshidrogenasa), mientras que en el irinotecan, su toxicidad se asocia con la deficiencia variable en glucoronosiltransferasa 1 (UGT1A1).
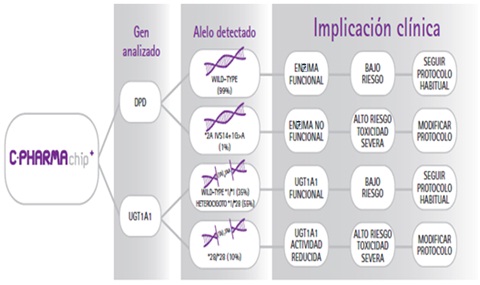
El C-PHARMA puede permitir al clínico predecir genéticamente la actividad metabólica de las enzimas implicadas en la eliminación de dichos fármacos, y contribuye en la elección del protocolo y la dosis más adecuada para ser administrada sin riesgo de toxicidad. Este bioanálisis fármacogenómico rastrea alelos del promotor, principalmente *1, *28, *36 y *37, del gen para la enzima UGT1A1 y el polimorfismo IVS14 + 1G>A o *2A de la enzima DPD. La detección de dichos polimorfismos contribuye a prevenir la aparición de toxicidad severa en los últimos estadios del cáncer de colon (III-IV); (Figura 1).
Figura 1. El C-PHARMAchip en Cáncer de Colon. Se ilustra el esquema comparativo de la implicación clínica de los hallazgos en los genes analizados mediante el test de C-PHARMAchip.
En el caso de aquellos pacientes a los que se les detecta que sean silvestres o normales, pueden ser candidatos para administrarles dosis con terapias que resultarán efectivas para combatir este grave y terrible padecimiento, mientras que a los que se les revelen genotipos poco favorables tienen la opción de someterse a tratamientos alternativos, evitando así perder tiempo, sufrimiento innecesario; a la par que se logra un mejor aprovechamiento del esfuerzo económico que estos tratamientos representan.
PERSPECTIVAS A FUTURO
Los bioanálisis genómicos de medicina personalizada tienen un enorme potencial para contribuir al cuidado de la salud y al combate a las enfermedades, no solamente en el caso de padecimientos graves, como este tipo de cáncer, sino también en otro tipo de patologías, que, cuando son diagnosticadas tardíamente o tratadas ineficazmente, merman la salud y por ende el bienestar de los mexicanos. Es, pues, imperativo practicarles tales análisis, para predecir la variabilidad genética que a cada paciente le hace reaccionar de manera específica y diferente a ciertos fármacos, para, en primera instancia, asistir a su médico en la elección del tratamiento y la dosis adecuada.
Hacer realidad la medicina personalizada en México no es únicamente tarea de investigadores de la genómica y de médicos avezados en estos avances, sino que es un esfuerzo de colaboración global para buscar hacer llegar cada día a más pacientes la oportunidad de beneficiarse de estos enfoques diagnósticos innovadores, que, como en el caso del cáncer de colon metastásico, revelan qué pacientes responderán más eficazmente y sin graves problemas de toxicidad a las mejores opciones terapéuticas que la medicina moderna les ofrece.
AGRADECIMIENTOS
Agradecemos a los pacientes, por su solidaria participación en estos estudios; a los médicos e instituciones colaboradoras, por sus invaluables apoyos, al facilitarnos biopsias de los pacientes; a Merck, por confiar en nosotros, para ofrecerles el servicio K-ras a los pacientes; a Progenika Biopharma, por compartirnos su experiencia sobre los microarreglos de diagnóstico, y a FONCICyT, por el apoyo económico para introducir estas pruebas a nuestro país en beneficio de pacientes mexicanos.
Literatura Consultada:
1. Wang H, Lopategui J, Amin M, Patterson S. KRAS Mutation Testing in Human Cancers: The Pathologist’s Role in the Era of Personalized Medicine. AdvAnatPathol 2010; 17; 23-32
2. Monzon F, Ogino S, Hammond E, Halling K, Bloom K, Nikiforova M. The Role of KRAS Mutations Testing in the Management of Patients With Metastásico Colorectal Cancer. Review Article. Arch Pathol Lab Med 2009; 133; 1600-1606
3. Jonssons M, Ekstrand A, Edekling T, Eberhard J, Grabau D, Borg D, Nilbert M. Experiences from treatment-predictive KRAS testing; high mutation frequency in rectal cancers from females and concurrent mutations in the same tumor. BMC Clinical Pathology 2009; 9: 8
4. Neuman J, Eberhart, Kirchner T, Jung A. Frequency and type of KRAS mutations in routine diagnostic analysis of metastatic colorectalcancer. Pathology – Research and Practice 2009; 858-862
5. Van Custem E, Lang I, D’haens G, Moiseyenko V, Zaluski J, Folprecht G, Tejpar S, Kisker O, Stroh C, Rougier P. KRAS status and efficacy in the first-line treatment of patients with metastatic colorectal cancer (mCRC) treated with FOLFIRI with or without cetuximab. J Clin Oncol; 2008; 26
6. Martinez S, Núñez A, Calderon A, Bosques F, Niderhauser A, Barrera H. Frequency and Clinicopathology Associations of K-ras Mutations in Colorectal Cancer in a Northeast Mexican Population. DigDis 1999;17:225-229.